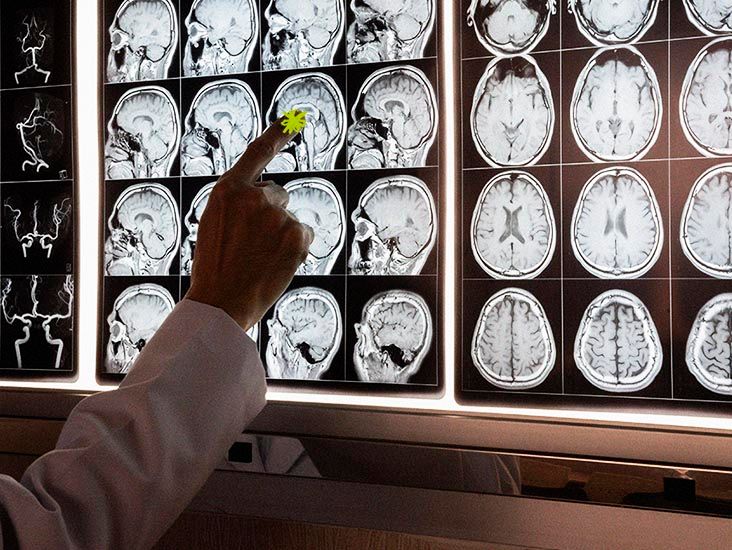
- في مرض الزهايمر، يؤدي تراكم بروتين تاو إلى موت أنسجة المخ.
- وقد ربط بحث جديد بين تراكم تاو وتراكم استرات الكولستريل، وهو شكل من أشكال الدهون المرتبطة بالالتهاب.
- وتشير النتائج إلى أن التخلص من استرات الكولسترول هذه قد يقلل من تلف الدماغ والتغيرات السلوكية التي تظهر لدى الأشخاص المصابين بمرض الزهايمر، على الأقل في الفئران حتى الآن.
- ومع ذلك، يؤكد الباحثون أن المركب المستخدم في دراستهم غير مناسب للاستخدام على البشر، لذلك يبحثون عن علاجات أخرى لها نفس التأثير المطهر.
مرض الزهايمر هو الشكل الأكثر شيوعا من الخرف، ويؤثر على أكثر من 6 ملايين شخص في الولايات المتحدة. مرض الزهايمر وأنواع الخرف الأخرى لها تأثير قريب
يُعتقد أن أعراض مرض الزهايمر، مثل فقدان الذاكرة والارتباك وتغيرات الشخصية، ترجع إلى حد كبير إلى تراكم غير طبيعي لاثنين من البروتينات في الدماغ —
الآن، وجدت دراسة أجريت على الفئران من قبل باحثين في كلية الطب بجامعة واشنطن في سانت لويس أن رواسب تاو في الدماغ مرتبطة بتراكم أحد أشكال الكوليسترول. عندما عولجت الفئران لتقليل استرات الكولسترول، انخفض أيضًا تلف الدماغ والتغيرات السلوكية.
يتم نشر البحث في المجلة الخلايا العصبية.
صميم البروتين الشحمي E (ApoE) هو بروتين موجود في الدماغ. فهو يساعد على تنظيم نقل الكولسترول وأنواع أخرى من الدهون في الدم. هناك
- قد يوفر APOE ε2 بعض الحماية ضد مرض الزهايمر. ما يقرب من 5% إلى 10% من الأشخاص لديهم هذا الأليل، مما قد يؤخر ظهور مرض الزهايمر أو حتى يمنعه.
- APOE ε3 هو الأليل الأكثر شيوعًا. وليس له أي تأثير على خطر الإصابة بالزهايمر.
- يزيد APOE ε4 من خطر الإصابة بمرض الزهايمر ويرتبط بالعمر المبكر لبداية المرض. حوالي 15% إلى 25% من الأشخاص لديهم هذا الأليل، و2% إلى 5% يحملون نسختين. إن وجود نسختين من هذا الأليل يزيد من خطر الإصابة بمرض الزهايمر أكثر من وجود نسخة واحدة.
أجرى الباحثون الدراسة الحالية على الفئران التي تم تعديلها وراثيا لتجميع بروتين تاو في دماغها. بحلول عمر 6 أشهر، بدأت هذه الفئران في تطوير علامات التنكس العصبي، وفي 9.5 أشهر، أصيبت بتلف شديد في الدماغ ولم تكن قادرة على القيام بأنشطة الفأر المعتادة، مثل بناء العش.
وقاموا أيضًا بتعديل الفئران عن طريق إزالة جينات APOE الخاصة بهم. إما أنهم استبدلوها بـ APOE ε3 أو APOE ε4 البشري، أو لم يستبدلوها.
“يوضح هذا البحث المثير للاهتمام العلاقة المعقدة بين Apolipoprotein E4 (ApoE4)، وهو عامل خطر وراثي مهم لمرض الزهايمر، وتراكم الدهون وأمراض تاو، في نموذج الفأر. إن اكتشاف الأساليب العلاجية المحتملة، مثل تعزيز تدفق الدهون الدبقية، يبشر بالخير لتدخلات محددة في مرض الزهايمر، مما يوفر الأمل في علاجات فعالة.
— الدكتور إيمر ماك سويني، الرئيس التنفيذي واستشاري أخصائي الأشعة العصبية في Re:Cognition Health، الذي لم يشارك في الدراسة.
في الفئران التي لديها أليل APOE ε4، تراكمت أيضًا مواد دهنية في مناطق الدماغ المتضررة، وخاصة استرات الكولستريل. معظم هذا التراكم الدهني كان موجودا
عندما تتراكم الخلايا الدبقية الصغيرة الكثير من الدهون، فإنها تبدأ في ذلك
“تصبح الخلايا الدبقية الصغيرة المليئة بالدهون شديدة الالتهاب وتبدأ في إفراز أشياء ليست مفيدة للدماغ.”
— الدكتور ديفيد إم هولتزمان، أستاذ باربرا بيرتون وروبن إم موريس الثالث المتميز في علم الأعصاب، جامعة واشنطن في سانت لويس، وكبير مؤلفي الدراسة.
استخدم الباحثون
بدءًا من عمر فئران تاو ستة أشهر، وهو العمر الذي يبدأ فيه التنكس العصبي عادة، أعطاها العلماء الدواء. بعد العلاج، عندما كان عمر الفئران 9.5 شهرًا، قاموا بتقييمها.
وبعد 9.5 شهرًا، كان لدى الفئران التي أعطيت الدواء حجم دماغ أكبر بكثير من تلك التي تلقت دواءً وهميًا. بالإضافة إلى ذلك، كان لديهم مستويات أقل من بروتين تاو، وعدد أقل من الخلايا الالتهابية، والتهاب أقل، وفقدان أقل للمشابك العصبية في أدمغتهم. كما احتفظوا بقدرتهم على بناء أعشاش أفضل من الفئران التي أعطيت العلاج الوهمي.
وبعد مزيد من البحث، وجد الباحثون أن ناهض LXR ينظم جينًا يسمى أبكا1 الذي يساعد على تحريك الكولسترول والدهون الأخرى خارج الخلايا.
“الأمر المثير هو أننا نرى كل هذه التأثيرات في نموذج حيواني يشترك في الكثير من الميزات مع الأمراض التنكسية العصبية البشرية. وقال الدكتور هولتزمان: “إن هذا يظهر أن هذا النوع من النهج يمكن أن يكون له الكثير من الأمل”.
وهذا النهج قد يفيد أكثر من الدماغ، كما قال الدكتور ماكسويني الأخبار الطبية اليوم:
“بالنظر إلى التشابه بين الآلية التي تدفع الخلايا المناعية المليئة بالدهون إلى إتلاف الدماغ والآلية التي تدفع الخلايا المناعية المحملة بالدهون إلى التسبب في تلف الأوعية الدموية في تصلب الشرايين، فإن الدواء الذي يمكنه إزالة الدهون في كلتا الخليتين يمكن أن يكون له تأثير مزدوج”. تأثير يفيد الدماغ والقلب والأوعية الدموية.
على الرغم من أن هذه الدراسة تظهر إمكانات العلاج، إلا أنه لا يمكن استخدامه على الأشخاص لأنه له آثار جانبية شديدة. تؤثر منبهات LXR على استقلاب الدهون في الكبد ويمكن أن تسبب مرض الكبد الدهني.
وقال الدكتور ماكسويني: “تتطلب المرحلة التالية حلاً لجعل هذا النوع المحتمل من العلاج غير سام للكبد لدى البشر”. إم إن تي.
“وهذا يمكن بدوره أن يمهد الطريق لدراسات بشرية مبكرة لاكتشاف ما إذا كان هذا العمل المبكر على الفئران يمكن أن يؤدي إلى علاج مطلوب بشكل خاص للأشخاص الذين يعانون من جين Apolipoprotein E4، الذين يحملون أعلى خطر للإصابة بمرض الزهايمر بين السنتين. الأعمار من 65 إلى 85 عامًا. وأضافت: “وكل من يعاني من مرض الزهايمر وربما تصلب الشرايين أيضا”.
أحد البدائل يمكن أن يكون الطرق الجينية. وتوصل البحث إلى أن زيادة
قال الدكتور هولتزمان: “أعتقد أن العلاج الجيني الذي يزيد من Abca1 في الدماغ يمكن أن يكون له تأثيرات مماثلة لإزالة الدهون”.
وأضاف الدكتور ماكسويني: “إنه وقت مثير لأبحاث مرض الزهايمر حيث نكتسب المزيد من المعرفة حول المرض ومسارات العلاج”.